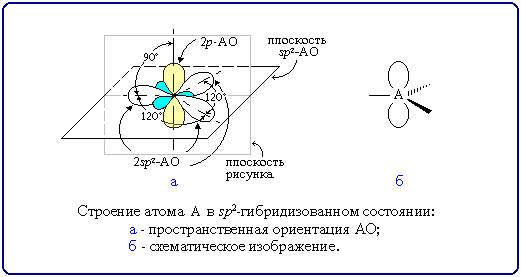
Как понять гибридизации в неорганике. Простое объяснение с примерами. Часть 3.
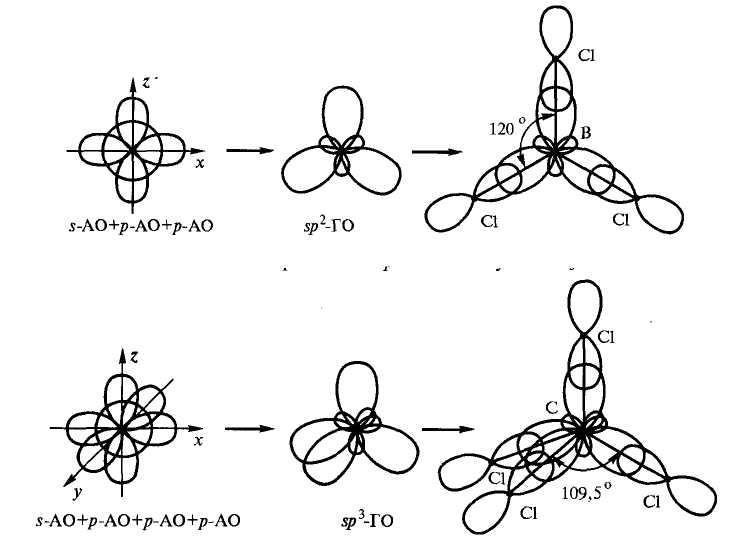
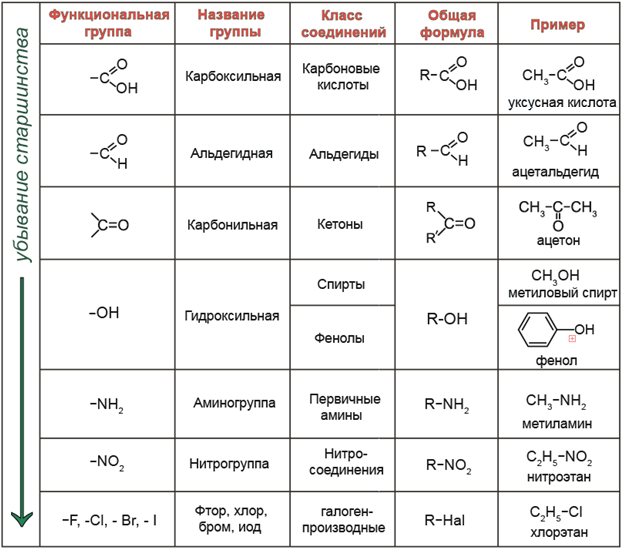
Часто химические связи образуются за счёт электронов, расположенных на разных атомных орбиталях. Казалось бы, и связи в молекуле по прочности должны быть неравноценными. Однако опыт показывает, что они равнозначны. Это явление объясняется представлением о гибридизации атомных орбиталей, введённым американским химиком Л. Рассмотрим образование молекулы метана.
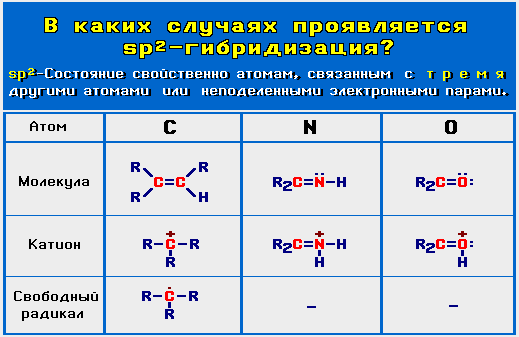
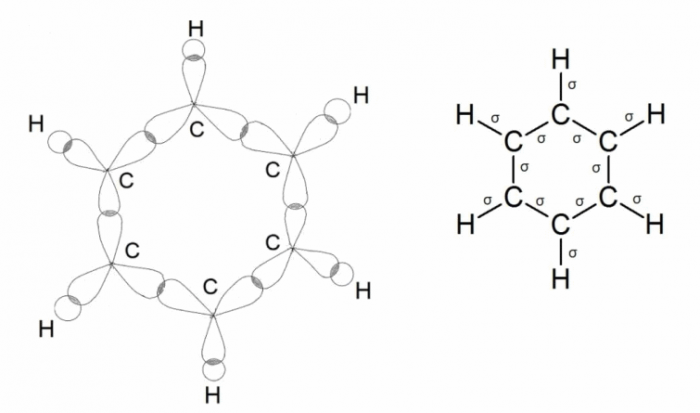


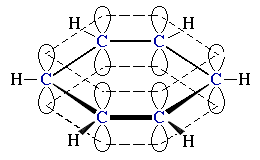


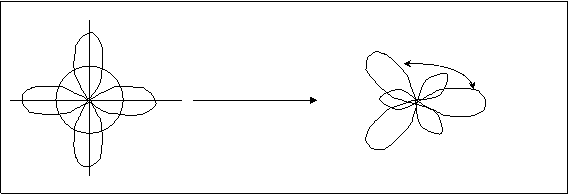


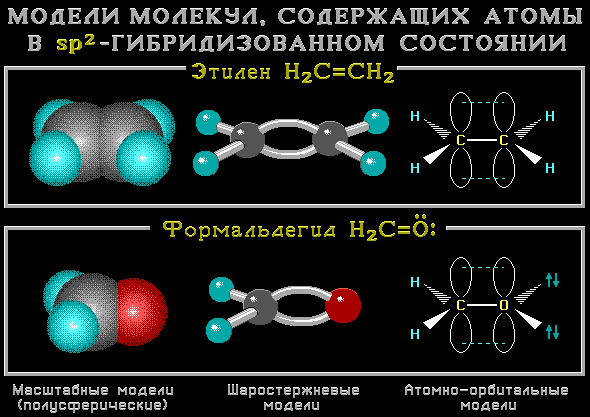
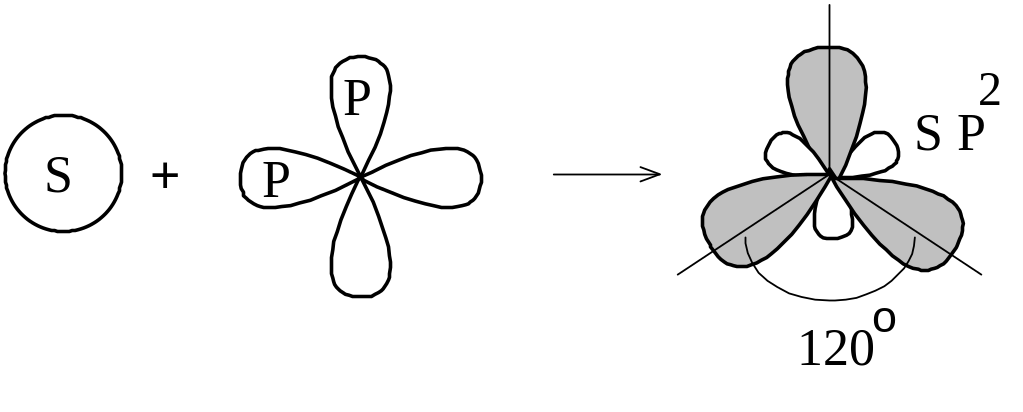
Чтобы войти в систему и использовать все возможности "Академии Хана", пожалуйста, включите JavaScript в своём браузере. Внести пожертвование Войти Зарегистрироваться Поиск курсов, уроков и видеороликов. Hybridization and hybrid orbitals. О проекте Об этом видео Транскрипция. Такая гибриизация возникает, когда атом окружён тремя группами электронов.
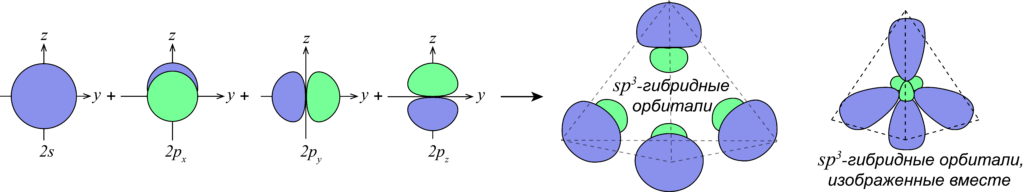


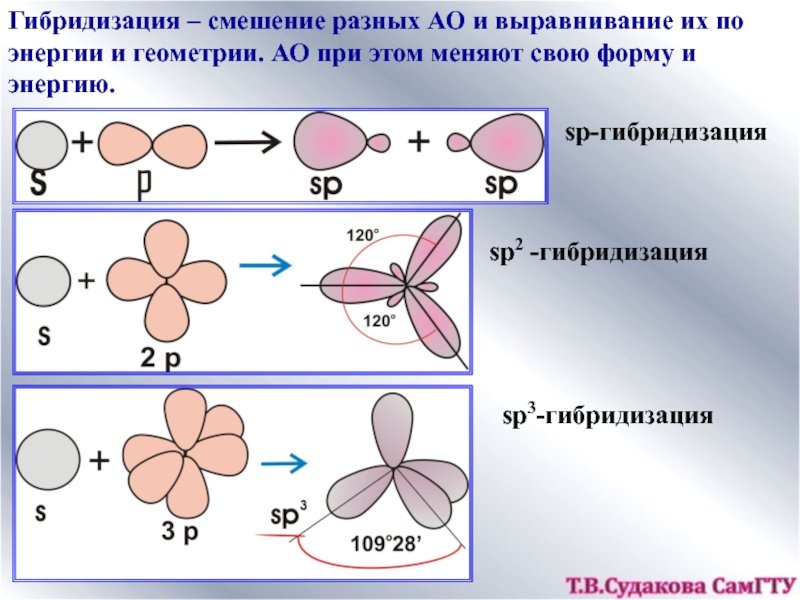
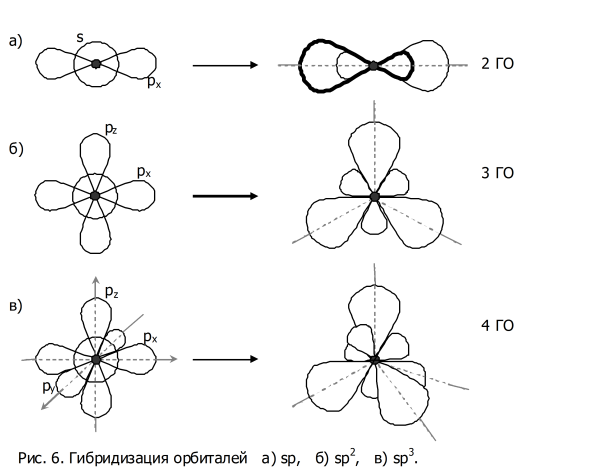

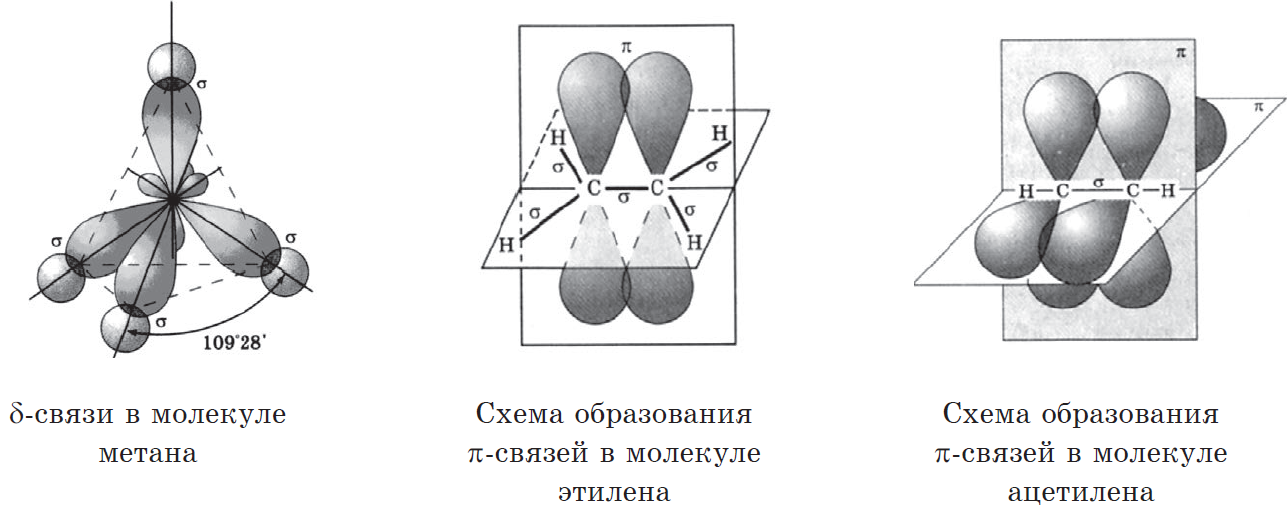

Понятие г ибридизации электронных орбиталей. Состояние валентных электронов описывает математическая модель гибридизации электронных орбиталей , которая предполагает не только выравнивание энергии, но и изменение формы орбитали, то есть смещение электронной плотности относительно ядра. Типы гибридизации атомов углерода. Понятие гибридизации электронных орбиталей впервые было введено Л. Полингом в г.